בשורה: חיישן המסמן גידולים סרטניים
חיישן חכם שפותח באוניברסיטת ת"א יאפשר למנתחים לזהות ולהסיר את כל תאי הגידול הסרטני. החיישן החדשני, מסמן את שולי הגידול באופן מדויק ביותר, תוך שהוא מאפשר פגיעה מינימלית בלבד ברקמות בריאות
קבוצת מחקר רב-תחומית בהובלת פרופ' רונית סצ'י-פאינרו, ראש המחלקה לפיזיולוגיה ולפרמקולוגיה בפקולטה לרפואה ע"ש סאקלר באוניברסיטת תל אביב, פיתחה חיישן ננומטרי חכם, שפועל כמתג המדליק אור פלואורסצנטי בנוכחות תאים סרטניים. החיישן מסמן את הגידול ואת שוליו ברמת דיוק גבוהה במיוחד, ובכך מאפשר למנתחים להסיר את הגידול במלואו - תוך פגיעה מינימלית ברקמות הבריאות סביבו, ומבלי להותיר בגוף תאים ממאירים, שעלולים להתפתח מחדש ו/או לשלוח גרורות קטלניות לאיברים אחרים. המשמעות: עלייה ניכרת באחוזי ההישרדות ובסיכויי ההחלמה של המנותחים.
את המחקר הובילו רחל בלאו, יאנה אפשטיין ויבגני פיסרבסקי, סטודנטים לדוקטורט ממעבדתה של פרופ' סצ'י-פאינרו. המחקר התפרסם במאי 2018 בכתב העת המדעי Theranostics.
פרופ' סצ'י-פאינרו מסבירה כי: "במחקר החדש התבססנו על מחקרים קודמים בהם גילינו מאפיין ייחודי של מגוון גידולים סרטניים: ביטוי מוגבר של אנזימים המכונים קטפסינים. תפקידם של אנזימים אלה, המצויים בכמות פחותה בהרבה גם בתאים בריאים, הוא לזהות ולחתוך רצף מסוים של חומצות אמינו (אבני הבניין של החלבונים). אנחנו ניצלנו את התכונה הזאת כדי לבנות חיישן חכם, שיזהה ויתייג תאים סרטניים."
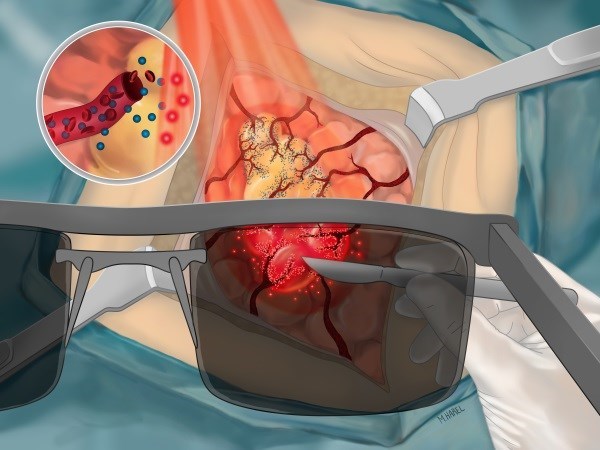
ניתוח לאחר הזרקה של חיישן חכם הזוהר בגידול ומסייע להבחין בין רקמה סרטנית לרקמה בריאה. איירה: מעין הראל
איך זה עובד?
החוקרים ייצרו ננו-חלקיקים פולימריים, המורכבים מאותו רצף חומצות אמינו שהקטפסינים נועדו לחתוך. החלקיקים הללו חוברו לתגים פלואורסצנטיים העשויים ממולקולות של חומר הצבע ציאנין (Cy). "כשמולקולות הציאנין מוחזקות יחדיו על ידי החלקיק הפולימרי, גלי האור שהן פולטות מבטלים זה את זה, והן נותרות חשוכות", אומרת פרופ' סצ'י-פאינרו. "אך ברגע שהננו-חלקיק מגיע לתא סרטני, הפולימר המחבר נחתך על ידי הקטפסינים, ומולקולות הציאנין מתרחקות זו מזו, ומאירות באור זוהר. לעומת זאת, ברקמה הבריאה שמסביב, הפולימר אינו נחתך, והאזור נותר חשוך. הגבול בין האזור המואר (הגידול) לחשוך (תאים בריאים) ברור מאוד לעין".
במונחים מקצועיים, המשמעות היא שלחיישן החכם יש רגישות גבוהה – הוא מגלה את כל התאים הסרטניים, ויש לו גם סלקטיביות גבוהה – הוא אינו מתייג תאים בריאים. בדרך זו הוא מדווח למנתח על מיקומם של התאים הסרטניים בזמן אמת, כלומר במהלך הניתוח עצמו - מתחת לסף הגילוי של אמצעי הדימות הקיימים כיום.
המחקר פורץ הדרך בוצע בשיתוף פעולה עם פרופ' צבי רם, ראש המחלקה לנוירוכירורגיה בבית החולים איכילוב, וסגניתו ד"ר רחל גרוסמן. בשלב הראשון הוכח כי האנזים המפעיל את החיישנים אכן קיים ומבוטא ביתר ברקמות שנכרתו מחולים בחדר הניתוח והועברו למעבדה. בהמשך נעזרו החוקרים במודלים של עכברים לסרטן השד ולסרטן העור מסוג מלנומה, שנוטים לשלוח גרורות למוח ולריאות. העכברים חולקו לשתי קבוצות עיקריות: חלקם נותחו להסרת הגידול תחת אור לבן רגיל, ללא עזרים נוספים, ואילו לקבוצה השנייה הוזרק החיישן החדש לפני הניתוח.
התוצאות היו מבטיחות ביותר: בעכברים שנותחו ללא החיישן אובחנו תוך זמן קצר גרורות או חזרה של הגידולים עצמם, ותוחלת החיים שלהם הייתה קצרה - רק 40% מהעכברים בקבוצה זו שרדו 120 יום לאחר הניתוח. לעומת זאת, כשהניתוח בוצע בעזרת החיישן החדש, שרידות העכברים הייתה כפולה: 80% מהם נותרו בריאים כעבור 120 יום. במילים אחרות: 60% מהעכברים שנותחו בניתוח 'הרגיל' מתו בסופו של דבר מהמחלה, בהשוואה ל-20% בלבד מאלה שנותחו באמצעות החיישן החכם.
בנוסף, הושווה החיישן החדש גם לשני חיישנים שנמצאים היום בניסויים קליניים בחדרי ניתוח. נמצא כי רמות הרגישות והסלקטיביות שלו גבוהות יותר, והוא אף נדלק הרבה יותר מהר. ברמה הטיפולית, המשמעות היא כי אין צורך לאשפז את המטופל יום קודם, ואפשר להזריק לו את החיישן רק כ-4 שעות לפני הניתוח.
"רשמנו מספר פטנטים על הפיתוח," מסכמת פרופ' סצ'י-פאינרו, "וכעת אנחנו מנהלים משא ומתן עם מספר חברות תרופות, במטרה להתקדם לשלב הניסויים הקליניים, ובהמשך לייצור בכמויות מסחריות. אנחנו מאמינים שהחיישן החכם שלנו יכול להביא לשיפור של ממש בתוצאות של ניתוחים להסרת גידולים סרטניים, ולהעלות משמעותית את סיכויי החולים לשרוד את המחלה".
במחקר זה השתתפו גם פרופ' דורון שבת מבית הספר לכימיה באוניברסיטת תל אביב ופרופ' גליה בלום מהפקולטה לרפואה באוניברסיטה העברית. מחקר זה מומן על ידי האיחוד האירופי (ERC), הקרן הלאומית למדע, משרד המדע והאגודה למלחמה בסרטן.
