בדיקת KRAS: גורמים אפשריים, מצבים דומים ומאמרים
 הכי חשוב לדעת על בדיקת KRAS
הכי חשוב לדעת על בדיקת KRAS
סרטן המעי: מרקרים גנטיים

סרטן במערכת העיכול: סכנה שקטה
איברי מערכת העיכול חשופים לסכנה של סרטן, וברוב המקרים אין תסמינים עד שהמחלה מתקדמת. טיפולים חדשניים מאפשרים לטפל בשלבי המחלה המאוחרים
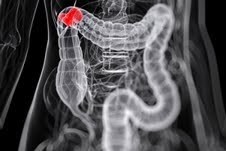
סרטן המעי: הבדיקה שאסור לשכוח
כמחצית מחולי סרטן המעי הגס אינם מודעים לקיומה של בדיקת סמן גנטי, הבוחנת את התאמתם לטיפול ביולוגי חדשני העשוי להביא לריפוי מלא
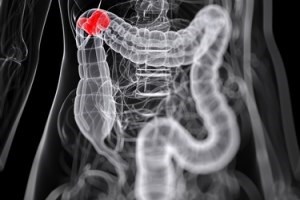
סרטן המעי: מרקרים גנטיים
אונקולוגיה מותאמת אישית מתבססת על ההבנה שיש שוני גנטי בין גידולים סרטניים. כך, ניתן להתאים טיפול אישי - ולהעלות משמעותית את סיכויי ההישרדות
צרכנות רפואית מס' 152
חדש בצרכנות: טיפול בסרטן השד, מוצרים לריפוי פצעים בפה, טיפול בסרטן מעי גס וערכה משופרת לחולי טרשת נפוצה
בדיקת KRAS: תשובות ממומחים וייעוץ אונליין
שלום ד"ר. אני מעוניינת לדעת כיצד פועלת בדיוק תרופת הארביטוקס כאשר מדובר בגידול ראש צוואר. כיצד היא תוקפת את הגידול? מה הוא מגנון הפעולה של התרופה? מה הקשר בין התרופה לבין הקולטן EGFR ואיך קשורה לכל זה בדיקת KRAS? כמו כן, כיצד נוטלים את התרופה? עירוי לוורידים? קפליות? שתייה? כל כמה זמן? יש מינון מומלץ? תודה.
ארניטוקס מעכבת בתאים את הקולטן ל EGFR (גורם לצמיחת התאים התפתחותם והתמיינותם). חסימת הקולטן תגרום להשתקת הסיגנל ולכן עצירת גדילת התא והרס שלו. התרופה ניתנת דרך הוריד פעם בשבוע. אין קשר עם K-ras בגידולי ראש צוואר (בניגוד למעי). המינון: 400מג בשבוע ראשון ו 250מג לאחר מכן. בהצלחה, ד"ר אבי חפץ, א.א.ג. יו"ר החברה לכירורגיה ואונקולוגיה של ראש צוואר בישראל, היחידה לכירורגיה ואונקולוגיה של ראש צוואר באסותא א.ר.ם.- המרכז לרפואת אאג וניתוחי ראש צוואר באסותא 03-7645464. www.aram-ent.co.il
לבעלי נתגלה סרטן הלבלב מסוג אדינוקרצינומה בשלב 4 לפני שנה, עם מחלות רקע של כולסטרול ויתר לחץ דם, מעשן, דרך החמרת סכרת וצהבת חסימתית הותקן לו סטנד מטאלי בתהליך ERCP. בפט סי.טי. מחודש 3/24 היתה קליטה פתולוגית היפודנסית בלתי מוגדרת כ-3.2 בראש הלבלב, וקליטה זעירה בזנב הלבלב, קליטה בכבד 0.9 ס"מ ובקשרית הלימפה של 0.6 ס"מ, בחודש זה התחלנו כימותראפיה FOLFOX. בפט סי.טי. מחודש 6/24 ללא עדות לקליטה מובהקת לגידול פעיל עם טיפול כימותראפיה FOLFIRINOX. כנ"ל גם בפט.סי.טי מחודש 8/24. בחודש 7/24 עבר מיפוי כליות DTPA עם FUSID מימין 47% משמאל 53%. מפיענוח NGS מולקולרי קצר, הודגמה מוטציה KRAS P, G12D, ללא עדות למוטציה נוספת. בפט.סי.טי מחודש 11/24 קליטה בראש הלבלב בולטת מבדיקה הקודמת בקוטר של 2 ס"מ ללא עדות לקליטה בכבד וללא עדות למימצא אחר. מבדיקת M.R.I. מ-11/24 תהליך הסננתי היפואינטנסי בראש הלבלב בגודל משוער כ-1.4 ס"מ הנראה כהופווסקולרי בשלב העורקי עם ביטוי ב-DWI קיימת אטרופיה של גוף וזנב הלבלב, הרחבה דיפוזית של צינור הלבלב לכל אורכו ברוחב מקסימלי עד 0.9 ס"מ שנראה ללא שינוי. הכבד בגודל וצורה ואותות תקינים ללא עדות לנגעים מוקדיים חשודים, סיימנו 12 פרוטוקולים של כימותראפיה. בסוף חודש 1/25 סיימנו חודש הקרנות בזיו בצפת ובע"ה באמצע 3/25 נבצע פט.סי.טי ובינתיים בעלי מקבל כימותראפיה FOLFOX במינון 50% ביצענו אקו לב דופלר, צילום חזה, ובדיקות ריאות. כל תקופת הטיפולים מרקר 19-9XR CA נע בין 2.06-8.05 ו-CEA 13.72-26.85. שאלותיי הן : האם כדאי לנתח ? מה הסטטיסטיקה לניתוח " וויפל " האם הניתוח הזה מומלץ לדעתך או האם אפשרי וכדאי יותר רק להוציא את הגידול ? מה הסטטיסטיקה להחלמה אחרי ניתוח " וויפל " או שאין כזאת ? האם תוחלת החיים גם אחרי ניתוח " וויפל " היא 5 שנים ? האם חלילה יש הישנות של סיכון מסוים שהמחלה עלולה לחזור ? והאם נסיגת המחלה נשמרת גם אחרי ניתוח ? האם אתה ממליץ על טיפול סיסטמי קבוע ? מאיזה משקל מנתחים ? בעלי שוקל 45 ק"ג היות והוריד קרוב ל-20 ק"ג ממשקלו, מדגישה שהוא עם מוטיבציה גבוהה בע"ה להחלים ומתפקד די טוב. תודה
שלום זה נושא מורכב יש לפנות למרפאה גסטרו ולהבדק במרפאה רפואה שלמה 🙏
לבעלי נתגלה סרטן הלבלב מסוג אדינוקרצינומה בשלב 4 לפני שנה, עם מחלות רקע של כולסטרול ויתר לחץ דם, מעשן, דרך החמרת סכרת וצהבת חסימתית הותקן לו סטנד מטאלי בתהליך ERCP. בפט סי.טי. מחודש 3/24 היתה קליטה פתולוגית היפודנסית בלתי מוגדרת כ-3.2 בראש הלבלב, וקליטה זעירה בזנב הלבלב, קליטה בכבד 0.9 ס"מ ובקשרית הלימפה של 0.6 ס"מ, בחודש זה התחלנו כימותראפיה FOLFOX. בפט סי.טי. מחודש 6/24 ללא עדות לקליטה מובהקת לגידול פעיל עם טיפול כימותראפיה FOLFIRINOX. כנ"ל גם בפט.סי.טי מחודש 8/24. בחודש 7/24 עבר מיפוי כליות DTPA עם FUSID מימין 47% משמאל 53%. מפיענוח NGS מולקולרי קצר, הודגמה מוטציה KRAS P, G12D, ללא עדות למוטציה נוספת. בפט.סי.טי מחודש 11/24 קליטה בראש הלבלב בולטת מבדיקה הקודמת בקוטר של 2 ס"מ ללא עדות לקליטה בכבד וללא עדות למימצא אחר. מבדיקת M.R.I. מ-11/24 תהליך הסננתי היפואינטנסי בראש הלבלב בגודל משוער כ-1.4 ס"מ הנראה כהופווסקולרי בשלב העורקי עם ביטוי ב-DWI קיימת אטרופיה של גוף וזנב הלבלב, הרחבה דיפוזית של צינור הלבלב לכל אורכו ברוחב מקסימלי עד 0.9 ס"מ שנראה ללא שינוי. הכבד בגודל וצורה ואותות תקינים ללא עדות לנגעים מוקדיים חשודים, סיימנו 12 פרוטוקולים של כימותראפיה. בסוף חודש 1/25 סיימנו חודש הקרנות בזיו בצפת ובע"ה באמצע 3/25 נבצע פט.סי.טי ובינתיים בעלי מקבל כימותראפיה FOLFOX במינון 50% ביצענו אקו לב דופלר, צילום חזה, ובדיקות ריאות. כל תקופת הטיפולים מרקר 19-9XR CA נע בין 2.06-8.05 ו-CEA 13.72-26.85. שאלותיי הן : האם כדאי לנתח ? מה הסטטיסטיקה לניתוח " וויפל " האם הניתוח הזה מומלץ לדעתך או האם אפשרי וכדאי יותר רק להוציא את הגידול ? מה הסטטיסטיקה להחלמה אחרי ניתוח " וויפל " או שאין כזאת ? האם תוחלת החיים גם אחרי ניתוח " וויפל " היא 5 שנים ? האם חלילה יש הישנות של סיכון מסוים שהמחלה עלולה לחזור ? והאם נסיגת המחלה נשמרת גם אחרי ניתוח ? האם אתה ממליץ על טיפול סיסטמי קבוע ? מאיזה משקל מנתחים ? בעלי שוקל 45 ק"ג היות והוריד קרוב ל-20 ק"ג ממשקלו, מדגישה שהוא עם מוטיבציה גבוהה בע"ה להחלים ומתפקד די טוב. תודה
התשובות לשאלותיך מורכבות. ראשית להבנתי הייתה גרורה אחת בכבד, ומאז האבחנה לא הופיעו גרורות רחוקות נוספות, להיפך, הגרורה בכבד כבר לא מודגמת בסיטי פרט. בנוסף, הגידול בראש הלבלב קטן באופן משמעותי, מה שמלמד שהוא מגיב טוב לטיפולים שהוא מקבל. יחד עם זאת, הוא שוקל 45 ק״ג מלמד שהוא במצב תזונתי ירוד. ניתוח וויפל הוא ניתוח המסיר את ראש הלבלב כולל הגידול שבו. זהו ניתוח גדול ומורכב ונושא סיבוכים ואף תמותה, ובעיקר במטופלים ירודים כמו בעלך, ולכן אני חושש שלא יעמוד בניתוח כזה. האם המחלה באמת נעלמה מהגוף? אני לא חושב, המחלה כעת לא נראית בלט סיטי, ואם יפסיק את הטיפול לזמן ארוך מידי היא עלולה לחזור. גידול של הלבלב בשלב 4 נחשב לגידול מתקדם. הייתי ממליץ להמשיך את הטיפול הכימוטרפי כל זמן שהוא משפיע. רפואה שלמה.
שלום דוקטור לפני חודשיים עברתי ניתוח בגלל גידול במעי הגס .בניתוח נמצא מלבד בלוטת לימפה אחת נגועה גם PELVIC NODULE שהוא היה סרטני ולכן הוגדרתי כ M1A .הומלץ לי על טיפול כימי משלים שאני נוטל אותו כבר חודשיים ומתוכנן שאני יקח עוד 3 חודשים .פט סיטי שעשיתי עכשיו חזר נקי ואין שום קליטות .בנתיים התעוררו אצלי ספיקות שכן בדבר נחיצות הטיפול משום שאני מבין שטיפול אדוגבנטי מטרתו הוא כשהמחלה היא מקומית ולא גרורתית למנוע את הפיכת המחלה לגרורתית אבל איך שאני קורא את מצבי אני גרורתי במצב יחודי של ללא עדות למחלה ולא בסטטוס של טיפול אדוגבנטי ואם כך יתכן שהפולפוקס שאותו אני לוקח הוא מיותר תודה רבה
אני חושבת שההחלטה במקרה של m1a ללא עדות למחלה לתת טיפול משלים היא מאוד נכונה. הסיכוי שיש מחלה מיקרוסקופית הינו גבוה והכימותרפיה אמורה לטפל בתאי סרטן אלה. בנוסף הייתי משלימה פרופיל מולקולרי כגון kras msih על מנת לקבל תמונה מלאה יותר. בהצלחה ובריאות שלמה שירה





